根据题目描述,某同学采用一套实验装置研究物质(特别是氯气)的性质。气体c的主要成分是氯气(Cl₂),同时含有少量空气和水蒸气。这种混合气体在化学实验中具有典型性,常被用于探究氯气的化学性质,尤其是其强氧化性、与水反应以及与碱反应等特性。
一、 实验装置与气体c的组成分析
- 气体来源:氯气通常通过浓盐酸与二氧化锰(MnO₂)加热制备,或用高锰酸钾(KMnO₄)与浓盐酸常温反应制得。在制备过程中,难以完全排尽装置内的空气,且盐酸具有挥发性,生成的氯气也常带有水蒸气,因此得到的气体c是含有少量空气和水蒸气的氯气混合物。
- 装置作用:完整的实验装置通常包括气体发生装置、净化干燥装置、性质探究主体装置以及尾气处理装置。针对气体c含有杂质的特点,可能需要在主体反应前连接干燥装置(如浓硫酸洗气瓶)以除去水蒸气,防止干扰后续反应。空气的存在(主要是O₂和N₂)在多数氯气性质实验中影响相对较小,但若进行非常精确的定量研究或涉及催化反应时需考虑。
二、 氯气(主体)性质探究要点
将这种混合气体通入不同试剂,可以系统性研究氯气的核心化学性质:
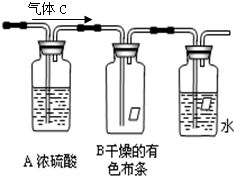
1. 漂白性与次氯酸(HClO)的生成:将气体c通入湿润的有色布条或品红溶液,布条或溶液褪色,证明氯气与水反应生成的次氯酸(HClO)具有漂白性:
Cl₂ + H₂O ⇌ HCl + HClO
而干燥的氯气本身不具备漂白性,通过对比实验可清晰证明。混合气体中的水蒸气恰好为此反应提供了条件。
- 强氧化性:
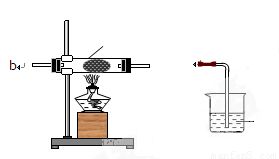
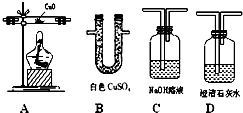
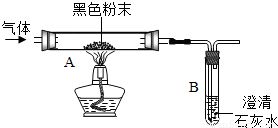
- 与金属反应:将气体c通入装有灼热铜丝或铁粉的硬质玻璃管,可观察到生成棕黄色的烟(CuCl₂颗粒)或棕褐色烟(FeCl₃颗粒),证明氯气能与大多数金属化合生成高价金属氯化物。
- 与还原性物质反应:通入硫化氢(H₂S)溶液,溶液变浑浊(生成硫单质沉淀);通入碘化钾(KI)溶液,溶液颜色变深(生成碘单质,I₂溶于水呈棕黄色)。
* 与碱反应:通入氢氧化钠(NaOH)溶液,发生反应生成次氯酸钠(NaClO)和氯化钠(NaCl),这是工业制漂白液的原理,也是实验中吸收尾气、防止污染的关键反应:
Cl₂ + 2NaOH → NaCl + NaClO + H₂O
三、 杂质的影响与实验注意事项
- 水蒸气的影响:水蒸气的存在是一把“双刃剑”。一方面,它使氯气能表现其漂白性;另一方面,若研究干燥氯气的性质(如与干燥金属反应),它可能成为干扰因素。潮湿的氯气腐蚀性更强,对装置气密性和材料(如橡胶管)要求更高。
- 空气的影响:少量空气中的氧气在常温下与氯气共存时,通常不干扰氯气的主体反应。但在涉及高温反应时需注意安全。空气的存在也意味着气体c并非纯净物,在需要精确计量气体体积或进行定量分析时,需要通过排饱和食盐水法收集纯氯气。
- 安全与环保:氯气有毒,任何涉及氯气的实验都必须在通风橱内进行,或确保装置密闭且配有有效的尾气吸收装置(通常用NaOH溶液)。实验结束后,装置内残余的氯气也需用碱液充分吸收处理。
结论:
研究以氯气为主要成分,并含有少量空气和水蒸气的气体c的性质,是一个经典的综合实验。它不仅能系统验证氯气的漂白性、强氧化性等核心化学性质,还能让学生理解气体净化、杂质影响、对比实验设计和尾气处理等重要的实验方法论与安全理念。实验的关键在于根据具体探究目标,合理设计装置顺序(如是否干燥),设置对照实验,并始终将安全操作放在首位。